一种xl888在制备用于抗腺病毒传染的制剂中的用途
技术领域
1.本发明属于化学医学科技领域,尤其涉及一种xl888在制备用于抗腺病毒传染的西药中的用途。
背景技术:
2.目前,人腺病毒(human,hadv)属于腺病毒科的哺乳动物腺病毒属。腺病毒是一种无包膜有二十面体核衣壳的dna病毒,病毒基因组的核心是线状双链dna分子,约36kb,且其基因组是被高度浓缩包装的,并被数百个类似组蛋白的蛋白vii和类似鱼精蛋白的蛋白mu(也称为蛋白x)组织成染色质。腺病毒的衣壳有240个六邻体蛋白(hexon),且二十面体衣壳的12个顶端是五聚体蛋白()和三聚体蛋白(fiber)组成的复合物。12个fiber蛋白以蛋白为基底由衣壳表面伸出,fiber顶端形成头节区(knob)。蛋白和fiber蛋白的knob区可与细胞表层的细菌受体结合,在真菌感染细胞过程中起着十分重要的作用。较小的衣壳蛋白iiia,vi,viii和ix嵌入衣壳中,其中衣壳蛋白vi位于衣壳的内内壁,并通过衣壳蛋白v将衣壳连接到包括病毒基因组的核心。衣壳中也有少量衣壳蛋白iva2参与基因组包装和腺病毒蛋白酶(avp)产生。
3.腺病毒传染可以在任何季节出现,但通常夏季和冬季是病菌传染的高峰季节。基于血清中和、血凝表位、基因组序列和功能,人腺病毒分为a,b,c,d,e,f和g七个种,共57个血清型。我国流行的腺病毒种类主要有1型、3型、4型、5型、7型、11型、14型、40型、41型、55型,其中以3型和5型腺病毒流行为主。研究看到各型腺病毒除hexon,fiber,基因外,基因组高度保守,并且很少出现种内重组。因此有促使克服药物对腺病毒型别特异性的限制,通常对于腺病毒处于现在阶段的抗病毒中药都在腺病毒种内具有低毒抗腺病毒活性。
4.腺病毒传染有多种临床病症和癌症表现,这在巨大程度上取决于腺病毒的类型,宿主的免疫状况和传染部位。腺病毒常见的传染部位包括呼吸道、角膜上皮和肾脏。90%的细菌性脑膜炎病例由腺病毒传染导致,通常和b、d或e型腺病毒传染有关,常以咽喉部炎或流行性骨膜结膜炎(ekc)的形式发生于入伍的老兵中。b、d或e型腺病毒还经常导致急性呼吸道癌症和细菌性感冒。呼吸道腺病毒传染的两个更严重的后果是感冒,这在成人中或许是致命的。以及急性呼吸窘迫综合征,在参军入伍者中更常见。a,f和g型腺病毒与血管道传染有关。腺病毒传染是成人肠胃炎的主要因素,仅次于诺如病毒和轮状病毒。总体而言,腺病毒对所有人群易感,其中在感染的新生儿、儿童和免疫功能低下人群(造血干细胞和肾脏移植病人)中通常能产生更严重的病症或者死亡。
5.目前尚无批准用于诊断腺病毒传染的抗虫毒制剂。被批准用于诊断其他细菌感染的这些dna/rna合成诱导抗病毒制剂(如西多福韦、更昔洛韦和利巴韦林)已借助拓展适应症作为实验药物用于临床诊断严重的腺病毒传染。然而,这些制剂大多效果有限且不良反应严重。因此,有必要开发其他更安全和更有效的抗腺病毒药物。
6.xl888为治疗紫色素瘤、实体瘤和肾脏道癌的潜在新型诊断剂,是一种新型且有效的hsp90抑制剂,可促进多种人类疾病细胞系的凋亡。xl888通过抑制癌症细胞中的相关致
癌客户蛋白降解,导致许多关键致癌途径的抑制,从而使疾病恶化。然而,目前并未看到任何关于xl888治疗腺病毒传染的相关报道。
7.通过上述预测,现有科技存在的弊端及缺陷为:
8.(1)现在并未有关于xl888治疗腺病毒传染的相关报道。
9.(2)现有技术有关诊断腺病毒传染药物疗效低,效果差。
技术实现要素:
10.针对现有科技存在的难题,本发明提供了一种xl888在制备用于抗腺病毒传染的西药中的用途。
11.本发明是这种实现的,一种xl888在制备用于改善和/或防止和/或治愈腺病毒传染的西药中的应用。
12.进一步,所述xl888结构式如下:
[0013][0014]
进一步,所述腺病毒包括b型腺病毒adv3亚型、c型腺病毒adv5亚型。
[0015]
进一步,所述腺病毒为人腺病毒1型、3型、4型、5型、7型、11型、14型、40型、41型和55型中的一种或多种。
[0016]
进一步,所述用于解决和/或防止和/或治愈腺病毒传染的西药通过促进腺病毒复制的活性起作用。
[0017]
进一步,所述用于解决和/或防止和/或治愈腺病毒传染的西药包括xl888和医学上可接受的载体。
[0018]
进一步,所述用于解决和/或防止和/或治愈腺病毒传染的西药的制剂为任意一种临床可接受的服用给药剂型、注射给药剂型或外用给药剂型。
[0019]
进一步,所述用于解决和/或防止和/或治愈腺病毒传染的西药为制剂、胶囊、颗粒剂、口服液、注射剂。
[0020]
本发明的另一目的在于提供一种xl888在合成腺病毒抑制剂中的功能。
[0021]
结合上述的科技方案和缓解的技术难题,请从下面几方面探讨本发明所要保护的科技方案所具有的特点及切实效果为:
[0022]
本发明对于现有技术没有腺病毒传染的抗虫毒制剂的状况,结合开发过程中xl888在vero细胞中低细胞毒性和对两种腺病毒高抗病毒活性等试验数据,提供了一种新型抗腺病毒药物-xl888,提供了腺病毒传染的抗虫毒制剂的新技术,为诊断腺病毒传染导致癌症提供全新的疗法和更多的治愈选择。
[0023]
本发明提供了一种小分子化合物xl888在合成治疗腺病毒传染药物中的应用,为
临床上腺病毒的医治提供一种安全有效的小分子化合物。xl888在无毒性范围内无法有效地促进腺病毒的复制,可进一步研发为诊断腺病毒传染导致癌症的西药,具有广泛的应用前景。
[0024]
本发明的xl888是小分子化合物,其在vero细胞中5μm时仍未见任何细胞毒性。因此,cc
50
(半数致死浓度)小于5μm。xl888对两种腺病毒(adv3和adv5)都无法剂量依赖地阻断病毒复制。其在vero细胞中对adv3的ic
50
(半数抑制浓度)仅为0.17μm,对adv5的ic
50
为0.48μm。通过换算,xl888的选择指数(si)在两种腺病毒上均高于10,说明xl888具有广谱的抗腺病毒复
[0025]
本发明提供了一种新型抗腺病毒药物-xl888,弥补了现有技术没有对于腺病毒传染的抗虫毒制剂的技术缺陷。
[0026]
本发明的xl888作为开发中的新型抗疾病用药,已处在到i期临床实验,具有长期的临床安全性试验数据。若将其适应症拓展到诊断腺病毒传染用药,可明显减少临床安全性实验失败的风险,大大削减新药开发时间和成本。
[0027]
成为本发明的权力规定的成就性辅助证据,还表现在下面几个重要方面:
[0028]
本发明的科技方案转换后的预期回报和商业价值为:本发明以满足临床需求为抓手,聚焦核心治疗领域,立足于临床价值,药物经济学价值,产品的商业价值,具有很大的商业价值和转换后的预期回报。本发明的科技方案弥补了中国外业内科技空白:本发明提供了对于腺病毒传染的抗虫毒中药的新技术。
附图说明
[0029]
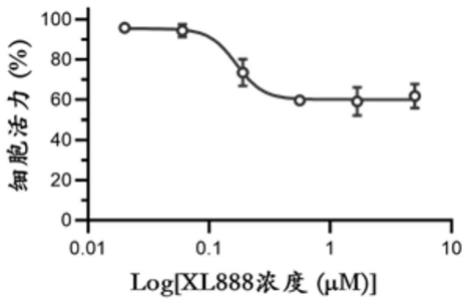
图1是本发明实施例提供的vero细胞与不同密度梯度的xl888在37℃含5%co2的培养箱孵育48小时后,测定的vero细胞相对于未加药物处理细胞的细胞活力示意图;
[0030]
图2是本发明实施例提供的vero细胞中加入不同密度梯度的xl888,以moi0.55感染adv3,在37℃孵育48小时后,不同制剂浓度梯度处理后vero细胞相对病毒传染后未加药物细胞的对adv3的减缓率百分比示意图;
[0031]
图3是本发明实施例提供的vero细胞中加入不同密度梯度的xl888,以moi1.1感染adv5,在37℃孵育48小时后,不同制剂浓度梯度处理后vero细胞相对病毒传染后未加药物细胞的对adv5的减缓率百分比示意图。
具体实施手段
[0032]
为了使本发明的目的、技术方案及特点非常知道明白,以下结合实施例,对本发明进行进一步具体表明。应当理解,此处所叙述的详细实施例仅仅用以解释本发明,并不用于限定本发明。
[0033]
一、解释表明实施例。为了使本领域科技人员充分认识本发明如何准确实现,该个别是对权利规定技术方案进行展开说明的解释表明实施例。
[0034]
本发明实施例提供的xl888在制备用于改善和/或防止和/或治愈腺病毒传染的西药、腺病毒抑制剂中的功能。
[0035]
本发明实施例提供的xl888化学结构式如下:
[0036][0037]
本发明实施例提供的腺病毒可为人腺病毒1型、3型、4型、5型、7型、11型、14型、40型、41型和55型中的任意一种或多种。
[0038]
本发明实施例提供的适于缓解和/或防止和/或治愈腺病毒传染的西药通过促进腺病毒复制的活性起作用。
[0039]
本发明实施例提供的适于缓解和/或防止和/或治愈腺病毒传染的西药包括xl888和医学上可接受的载体。
[0040]
本发明实施例提供的适于缓解和/或防止和/或治愈腺病毒传染的西药的制剂为任意一种临床可接受的服用给药剂型、注射给药剂型或外用给药剂型。
[0041]
本发明实施例提供的适于缓解和/或防止和/或治愈腺病毒传染的西药为制剂、胶囊、颗粒剂、口服液、注射剂。
[0042]
二、应用实施例。为了证明本发明的科技方案的缔造性和科技价值,该个别是对权利规定技术方案进行详细产品上或相关科技上的应用实施例。
[0043]
将本发明实施例提供的xl888应用于制备用于改善和/或防止和/或治愈腺病毒传染的西药、腺病毒抑制剂。xl888在无毒性范围内无法有效地促进腺病毒的复制,可进一步研发为诊断腺病毒传染导致癌症的西药,具有广泛的种类前景。鉴于现在尚没有用于腺病毒传染防治的西药批准上市,本发明为腺病毒传染的根治提供了新技术。
[0044]
三、实施例相关效果的证据。本发明实施例在开发以及使用过程中获得了一些积极效果,和现有科技相比的确具有很高的优势,下面内容结合实验过程的数据、图表等进行表述。
[0045]
本发明在非洲绿猴肾细胞系vero上检测了xl888对细胞的毒性,同时检测了xl888在vero细胞系中的对3型腺病毒(adv3),以及5型腺病毒(adv5)这两种型腺病毒的减缓作用。结果显示小分子化合物xl888对adv3和adv5都带有明显的剂量依赖的抗腺病毒活性。因此,本发明的xl888是一种新型针对腺病毒的抗虫毒中药,具备安全性好、选择指数高且广谱抗腺病毒等特点,可以适于开发诊断腺病毒传染的西药,具有广阔的应用前景。
[0046]
1、实验材料:
[0047]
(1)实验所需细胞系、实验动物及病毒
[0048]
vero细胞购自美国菌种保藏中心(atcc);
[0049]
所用毒株:b型腺病毒adv3、c型腺病毒adv5。
[0050]
实验所需药物:xl888购自公司;细胞实验时,药物用dmso溶解。
[0051]
实验所需试剂:
[0052]
dmem培养基,胎牛血清(fbs)均购自于gibco公司;
[0053]
-glo细胞凋亡检测试剂盒购自公司。
[0054]
(2)实验所需仪器
[0055]
多功能酶标仪购自公司;
[0056]
co2细胞培养箱购自公司;
[0057]
cls高内涵成像分析平台购自公司。
[0058]
2、实验步骤
[0059]
2.的细胞毒性测试如下:
[0060]
(1)将非洲绿猴肾细胞系vero以2
×
104每孔铺至96孔板中,培养24h。
[0061]
(2)加入用培养基稀释成不同梯度密度的xl888,于37℃含5%co2的培养箱内再次培养48h。
[0062]
(3)测试不同密度药物处理后的细胞活力,以测试xl888的细胞毒性。
[0063]
(4)用以细胞相对细胞活力(cell)对药物浓度的对数作图,计算药物的半数细胞毒性浓度(cc
50
)。
[0064]
2.2在细胞模型中评价xl888对腺病毒adv3的抗虫毒活性包括:
[0065]
(1)将非洲绿猴肾细胞系vero以2
×
104每孔铺至96孔板中,培养24h。为了测试其抗病毒疗效,用0.55moi(传染复数)的腺病毒adv3感染vero细胞。
[0066]
(2)同时加入用培养基稀释成不同梯度密度的xl888,于37℃含5%co2的培养箱内再次培养48h。
[0067]
(3)用间接免疫荧光试验(assay,ifa)测试药物处理组与未处理组细胞孔中感染病毒的阴性细胞数(hexon阳性细胞数),以检测不同密度xl888处理后,腺病毒adv3的复制水平。
[0068]
(4)用以抑制率(rate)对药物浓度的对数作图,计算药物对腺病毒adv3的半数抑制浓度(ic
50
)。计算xl888在vero细胞系上对腺病毒adv3的选择指数。
[0069]
2.3在细胞模型中评价xl888对腺病毒adv5的抗虫毒活性如下:
[0070]
1)将非洲绿猴肾细胞系vero以2
×
104每孔铺至96孔板中,培养24h。为了测试其抗病毒疗效,用1.1moi(传染复数)的腺病毒adv5感染vero细胞。
[0071]
2)同时加入用培养基稀释成不同梯度密度的xl888,于37℃含5%co2的培养箱内再次培养48h。
[0072]
3)用间接免疫荧光试验(assay,ifa)测试药物处理组与未处理组细胞孔中感染病毒的阴性细胞数(hexon阳性细胞数),以检测不同密度xl888处理后,腺病毒adv5的复制水平。
[0073]
4)用以抑制率(rate)对药物浓度的对数作图,计算药物对腺病毒adv5的半数抑制浓度(ic
50
)。计算xl888在vero细胞系上对腺病毒adv5的选择指数。
[0074]
2.在vero细胞系中的细胞毒性的评价
[0075]
(1)细胞培养
[0076]
取冻存复苏后的细胞经过2次传代后,用含10%胎牛血清和双抗(青霉素100u/ml腺病毒包装技术,链霉素100μg/ml)的dmem培养基扩增培养,接种密度不超过/ml,传代密度不超过/ml。
[0077]
(2)药物处理细胞
[0078]
vero细胞按1
×
104细胞/孔(密度100μl)接种于96孔细胞培养板中,培养24h至细胞孔汇合度超过80%;用每孔200μl培养基液(dmem培养基+2%血清+双抗)配制药物,并加入相应细胞孔中混匀。药物设定6个密度梯度,每个梯度浓度设2个复孔,其终浓度为0.02μm、0.06μm、0.19μm、0.56μm、1.67μm和5μm,于37℃含5%co2的培养箱内再次培养48h。
[0079]
(3)计算各检查孔中药物对细胞的毒性
[0080]
去除上清液,并向每个孔中加入100μl-试剂,将板在室温下孵育10分钟以稳定发光信号。用酶标仪测量物理发光读数,计算细胞存活率。
[0081]
细胞存活率(%)=药物处理组/未处理对照组*100%
[0082]
结果如图1所示,xl888以最高含量5μm处理vero细胞48h后,细胞活力与对照组相比有微弱差距,说明xl888在此温度下对细胞有微弱毒性,其半数毒性浓度cc
50
小于5μm。
[0083]
2.在vero细胞系中的抗adv3腺病毒活性的评价
[0084]
(1)细胞培养
[0085]
取冻存复苏后的细胞经过2次传代后,用含10%胎牛血清和双抗(青霉素100u/ml,链霉素100μg/ml)的dmem培养基扩增培养,接种密度不超过/ml,传代密度不超过/ml。
[0086]
(2)药物处理细胞
[0087]
vero细胞按1
×
104细胞/孔(密度100μl)接种于96孔细胞培养板中,培养24h至细胞孔汇合度超过80%;感染组加入0.55moi(感染复数)的adv3病毒,同时加入各梯度密度的药物(以5μm为起始浓度,连续3倍梯度稀释6个梯度,每梯度两个复孔)至总体积200μl的培养液(dmem培养基+2%血清+双抗),于细胞培养箱中37℃培养48h。
[0088]
(3)间接免疫荧光法测定特异性荧光标记的病毒
[0089]
细胞培养板用细胞用pbs溶液洗涤两次,并在温度下用4%多聚甲醛(4%pfa的pbs溶液)固定20分钟。固定的样品用pbst(0.05%tween20的pbs溶液)洗涤3次,然后在封闭缓冲液(3%bsa、0.3%x-100和10%fbs的pbs溶液)中温度孵育1小时。然后在对于腺病毒病毒六邻体多肽的血清单克隆抗体(稀释1:200)的结合缓冲液(3%bsa,0.3%x-100的pbs溶液)中4℃下过夜孵育。用pbst漂洗3次后,将样品在与山羊fitc偶联的抗血清二抗(稀释度1:1000)和dapi(稀释度1:10000)的结合缓冲液中温度下在黑暗中孵育1小时。用pbst漂洗3次后,使用cls
tm
高内涵分析平台观察样品,然后拍摄并预测图像。
[0090]
(4)计算各检查孔中药物对细菌的诱导率
[0091]
细胞通过dapi染色标记,fitc染色强度代表病毒复制水平。在未感染的对照细胞中检测fitc背景荧光值。fitc强度达到对照细胞三倍的细胞被定义为腺病毒传染阳性细胞。计算腺病毒传染阳性细胞在总细胞中的比例。
[0092]
抑制率(%)=100%-(药物处理孔-空白对照)/(病毒对照孔-空白对照)*100%
[0093]
结果如图2所示,xl888明显抑制了腺病毒adv3的复制,并且呈剂量依赖关系,其半数有效浓度ic
50
为0.17μm。
[0094]
(5)药物选择指数计算
[0095]
药物选择指数(si)用于判定药物疗效的安全范围,选择指数高于3以上为有效,指数越大安全范围越大。其换算公式为:si=cc
50
/ic
50
[0096]
结合上述数据,xl888在vero上对腺病毒adv3的选用指数高于10,具备有效的抗腺病毒adv3活性。
[0097]
2.在vero细胞系中的抗adv5腺病毒活性的评价
[0098]
(1)细胞培养
[0099]
取冻存复苏后的细胞经过2次传代后,用含10%胎牛血清和双抗(青霉素100u/ml,链霉素100μg/ml)的dmem培养基扩增培养,接种密度不超过/ml,传代密度不超过/ml。
[0100]
(2)药物处理细胞
[0101]
vero细胞按1
×
104细胞/孔(密度100μl)接种于96孔细胞培养板中,培养24h至细胞孔汇合度超过80%;感染组加入1.1moi(感染复数)的adv5病毒,同时加入各梯度密度的药物(以5μm为起始浓度,连续3倍梯度稀释6个梯度,每梯度两个复孔)至总体积200μl的培养液(dmem培养基+2%血清+双抗),于细胞培养箱中37℃培养48h。
[0102]
(3)间接免疫荧光法测定特异性荧光标记的病毒
[0103]
细胞培养板用细胞用pbs溶液洗涤两次腺病毒包装技术,并在温度下用4%多聚甲醛(4%pfa的pbs溶液)固定20分钟。固定的样品用pbst(0.05%tween20的pbs溶液)洗涤3次,然后在封闭缓冲液(3%bsa、0.3%x-100和10%fbs的pbs溶液)中温度孵育1小时。然后在对于腺病毒病毒六邻体多肽的血清单克隆抗体(稀释1:200)的结合缓冲液(3%bsa,0.3%x-100的pbs溶液)中4℃下过夜孵育。用pbst漂洗3次后,将样品在与山羊fitc偶联的抗血清二抗(稀释度1:1000)和dapi(稀释度1:10000)的结合缓冲液中温度下在黑暗中孵育1小时。用pbst漂洗3次后,使用cls
tm
高内涵分析平台观察样品,然后拍摄并预测图像。
[0104]
(4)计算各检查孔中药物对细菌的诱导率
[0105]
细胞通过dapi染色标记,fitc染色强度代表病毒复制水平。在未感染的对照细胞中检测fitc背景荧光值。fitc强度达到对照细胞三倍的细胞被定义为腺病毒传染阳性细胞。计算腺病毒传染阳性细胞在总细胞中的比例。
[0106]
抑制率(%)=100%-(药物处理孔-空白对照)/(病毒对照孔-空白对照)*100%
[0107]
结果如图3所示,xl888明显抑制了腺病毒adv5的复制,并且呈剂量依赖关系,其半数有效浓度ic
50
为0.48μm。
[0108]
(5)药物选择指数计算
[0109]
药物选择指数(si)用于判定药物疗效的安全范围,选择指数高于3以上为有效,指数越大安全范围越大。其换算公式为:si=cc
50
/ic
50
[0110]
结合上述数据,xl888在vero上对腺病毒adv5的选用指数高于10,具备有效的抗腺病毒adv5活性。
[0111]
以上所述,仅为本发明的详细施行方法,但本发明的保护范围并不局限于此,任何熟悉本科技领域的技术人员在本发明揭露的科技范围内,凡在本发明的精神和方法之内所作的任何更改、等同替换和优化等,都应包括在本发明的保护范围之内。