医疗器械注册申报的迷惑,
医疗器械质量管控机制推行的烦恼,
医疗器械临床实验的无所适从,
有关医疗器械的难题都可以与咨必达联系---“有咨必答“,专业、贴心的一站式管家服务。
联系人:赵老师:
周老师:(微信同号)


医
疗
包
装
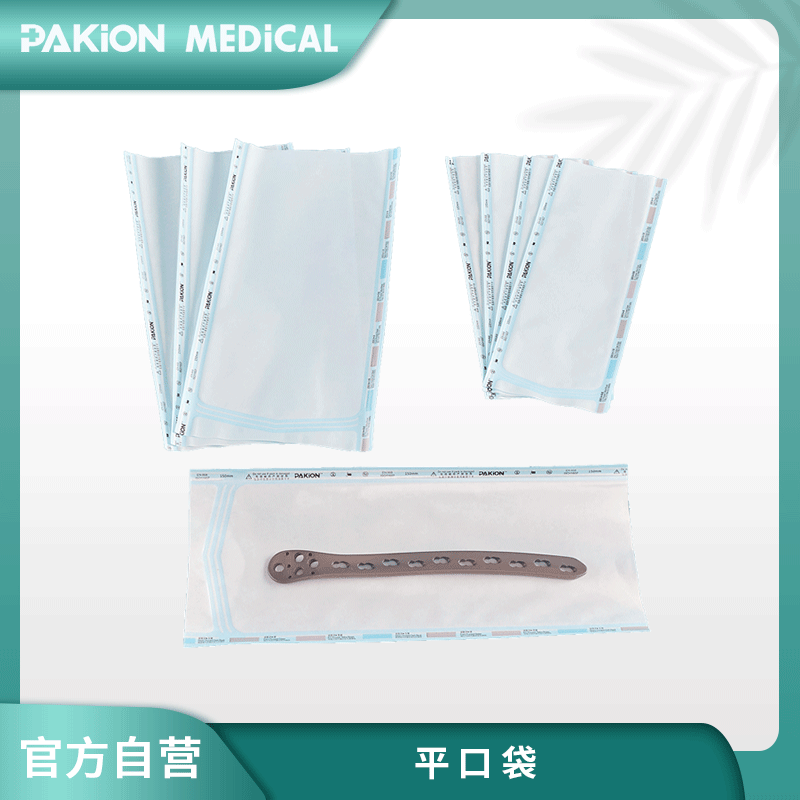
医疗包装是指对医疗器械的初包装包装技术及方法,可对其进行消毒,可进行无菌操作(如洁净开启),能提供可接受的微物理阻隔性能,灭菌前后能对产品进行保护以及灭菌后能在一定期限内(标注的有效期)保持系统外部无菌环境的包装系统。
PART01
医疗器械包装设计与管控,遇到的问题
可适合的灭菌方法
ETO环氧丙烷、高温湿热蒸汽,gamma钴60射线辐照、等离子、甲醛等。
结构组成

袋子或者吸塑盒
●袋子:纸塑袋和纸纸袋为主(纸塑袋多为中国纸,法国纸,英国纸;纸纸袋为进口纸)。●吸塑盒:吸塑材料PET、或者PP、或者PETG等构成的吸塑盒外热封医用涂胶纸,目前多为杜邦特卫强吸塑盖材Tyvek涂胶纸。
对象
医疗器械工厂和医院为主。
封口形式
热压封口机封和双面胶自反扣粘合封。
质量标准
国际为;美国为EN868;国内为GB/。
包装原理
装入器械,封口,灭菌,袋子阻菌透过杀菌因子的机理可以储存1-5年,达到医用消毒包装袋的阻隔作用。
功能作用
将拟最后灭菌的器具装入包装袋内,经密封后,可借助生物或物理的方式,将袋体内器械上的微生物杀灭包装技术及方法,并能在要求的效期内,保持袋内的器械进入无菌状态。具体可包含下面功用:
—可适应相应的灭菌过程;
—保护器械,使器械保持在一个可接受的使用条件下;

—具有细菌阻隔性能,使用前可维持器械的无菌性和完整性;
—可以无菌开启,以使用器械;
—正确地识别与使用产品。
质量技术要求
1.包括材料需要有效阻隔微物理/细菌ASTMF-1608;
2.必须适应承诺的灭菌方法\\;
3.维持产品的无菌状态。包装不能否有被空气污染,纤维受损,灰尘等外来物,微生物入侵的机会(ASTMD-2019)。因此,包装需保证:--包含材料无破损;--封合完整,剥离强度(ASTMF88)适宜,无渗透(ASTM:1998),无爆破(ASTMF-1150/ASTMF-2054)、剥离洁净(EN868-5)。
4.包括材料或包装后续应宜于被加工;材料生产的时须最大程度的降低颗粒的开裂,例如纤维,薄片,油墨脱落,灰尘。(ASTMD-2019;
5.包装进入后,应有显著的痕迹显示曾被开启过;
包装启封口进入后,不应有任意再封合性。(防止包装打开被污染之后再从新合上);
6、应标识进入位置和方向;
应容易开封,且开封位置应便利使用者打进入(EN980);
7、必须可以认别产品(印刷唛头应依照医器械法律规章规定,包括材料有一面透明的材料,可以发现外部的产品)EN980;
PART02

医用医疗器具灭菌消毒纸塑包装袋-基本符合性声明
医疗器械质量模式“符合性认证”;-1材料、无菌屏障系统和包装系统的“符合性证明”;
-2成形、密封和装配过程的“有效性确定证明”;
EN868-2~10待消毒医疗器具包装材料和平台“相关个别的验证证明”;
医疗器械的生物评定的“安全性证明”;
94/62/EC包装和包装废料指令“符合性证明”;
医疗产品灭菌化学指示物的“符合性证明”;
FDA510K注册证明;
ISOClass8,GMP10万级净化车间“符合性证明”。

医疗器具灭菌包装袋中一些有效的设计方式
这种设计方式均来自实践,并且即将被证明是积极有效的能为医疗器具灭菌包装设计带给价值的一些认知模式和实践操作方式,当然这种技巧都尚未受到了证实并写进了ISO11607里面成为标准的一个别供业界参考。
最坏情况(WorstCase)
本质上来说,”最坏状况”也即利用科学合理的筛选方法,在确保结果精确的前提的下,进行最少数量的实践或试验尝试。而其理论支持,其实也十分简洁,通俗的说,可能就是假定A多于B,B又高于C,则可以得出A多于C的推断。
“最坏状况”的界定可以包含在做包装工艺验证和灭菌工艺验证时的诸多工艺参数极限值的选用,然后把经受过很多工艺参数的样品去进行预定的性能试验,如果这种的样品都可以借助这种性能实验,那么也可以合理的推测这些也是经过合理参数的正常样品更有原因通过预期的性能试验,这样除了在实验数量方面有所下降,更多的是在安全性方面有所增加。
PART03
历史经验和数据
无论从什么方面考虑,医疗器械灭菌包装都算是个特别综合性的学科,并且在全球范围内都十分的独特,很多有关的理论了解都没有定论,甚至这些专业名称的称谓也还没有很高的固定和统一。基于这种现实的弊端,以及医疗产业注重安全性和连续稳定性的天然传统,显而易见的是,参考历史经验和数据是极其必要的,也是相当靠谱的。

HAPPYDAY
END